Durchführung von Mikrobiomanalysen zur Erfassung der gesamten bakteriellen Flora
Die Besiedlung des menschlichen Darms mit Billionen von Mikroorganismen beeinflusst den Gesamtorganismus auf vielfältige Art und Weise. So unterstützt das intestinale Mikrobiom nicht nur die effektive Verwertung von Nahrungsbestandteilen, sondern gewährt auch einen effektiven Schutz vor gastrointestinalen Infektionskrankheiten. Das Mikrobiom eines Menschen ist individuell zusammengesetzt und hängt vermutlich vor allem von genetischen Faktoren und vielen Umweltfaktoren ab. Jedes physiologisch zusammengesetzte Mikrobiom erfüllt lebenswichtige Funktionen, z.B. als wichtige lokale Barriere gegen bakterielle Krankheitserreger oder als Energielieferant aus für den Körper selbst unverdaulichen Zuckern Fetten und Ballaststoffen. Studien der letzten Jahre haben zudem gezeigt, dass Fehlbesiedlungen und Veränderungen in der Bakterienvielfalt mit dem Auftreten verschiedenster chronischer Erkrankungen wie z.B. Morbus, Crohn, Colitis Ulcerosa, Arthritis, Diabetes und neurologischen Erkrankungen assoziiert sind.
Unsere Forschungsabteilung untersucht die Zusammensetzung der Darmflora von Patienten und erforscht die Rolle des Mikrobioms bei der Krankheitsentstehung. Zur Sequenzierung und bioinformatischen Analyse der bakteriellen Flora von Patienten haben wir in den vergangenen Jahren eine spezielle Technologieplattform aufgebaut (Mikrobiomanalyse-Labor). Auf Anfrage und auf Kooperationsbasis bestimmen wir die Zusammensetzung der Bakterienflora im Stuhl und in Gewebeproben.
Sequenzierung des Mikrobioms

Neu entwickelte DNA-basierte Untersuchungstechniken und dabei insbesondere Fortschritte in der Hochdurchsatzsequenzierung eröffnen die Möglichkeit, die komplexe Bakterienvielfalt weitaus umfassender zu beschreiben als klassische kulturbasierte Verfahren. Wir verwenden für die Mikrobiomanalysen die MiSeq Plattform der Firma Illumina, die eine schnelle und qualitativ hochwertige Generierung von Millionen von Sequenzinformationen ermöglicht. Dabei werden variable Sequenzregionen des 16S rRNA Gens (Bakterien) oder der ITS1/ITS2 Region (Pilze) als Markergene verwendet, die in genomischer DNA z.B. von Stuhlproben sequenziert werden.
Bioinformatische Analyse des Mikrobioms
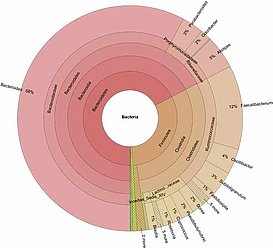
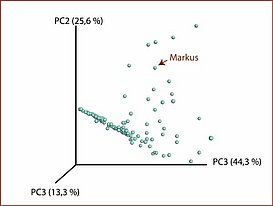
Über die bioinformatische Analyse dieser grossen Mengen an Sequenzinformationen stehen verschiedene Methoden zur Verfügung, die komplexe Zusammensetzung des Mikrobioms qualitativ und quantitativ zu beschreiben. So liefert die Bestimmung der „alpha“ Diversität Aussagen über den Artenreichtum im Mikrobioms, wohingegen Algorithmen zur Bestimmung der beta-Diversität den Vergleiche innerhalb experimenteller Gruppen und z.B. anderen Patientenkollektiven in Datenbanken ermöglicht.
Kontaktanfrage
Ansprechpartner:
PD. Dr. Stefan Wirtz
Medizinische Klinik 1
Hartmannstrasse 14
91052 Erlangen
stefan.wirtz@uk-erlangen.de
09131 85 35882/35960