Arbeitsgruppe Prof. Dr. rer. nat. Christoph Becker
Immunregulation der Epithelzellbarriere im Darm
Der Darm - Ein Organ mit vielen Superlativen
Unser Darm ist ein unglaublich faszinierendes Organ. Neben der Versorgung unseres Körpers mit Nährstoffen ist der Darm auch ein sehr wichtiges Organ für unser Immunsystem. Wusstest du, dass sich im Darm die meisten Immunzellen unseres Körpers befinden? Der Grund dafür ist, dass der Darm die größte Grenzfläche unseres Körpers zur Außenwelt darstellt. Über ihn steht der Darm in ständigem Kontakt mit den Bestandteilen der Nahrung und den Bakterien der Darmflora.
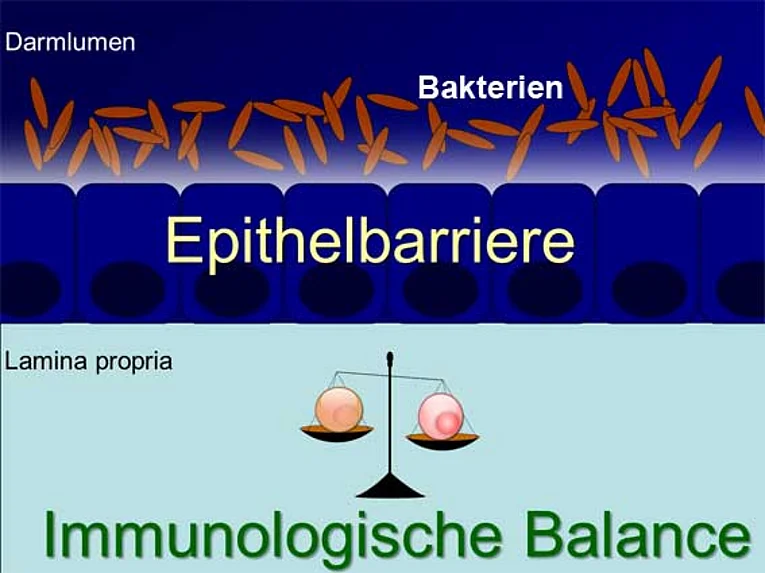
Die äußerste Grenzschicht wird von Epithelzellen gebildet, deren Aufgabe es ist, einerseits die Aufnahme von Nährstoffen aus der Nahrung zu gewährleisten, andererseits aber das unkontrollierte Eindringen von Stoffen in den Körper zu verhindern. Die Epithelzellen stellen somit eine Art gut bewachte Grenze dar. Unterhalb der Epithelzellen, tiefer in der Darmwand, befinden sich die Zellen des Immunsystems der Darmschleimhaut. Diese Zellen haben die wichtige Aufgabe, die aufgenommenen Stoffe aus der Nahrung und die Bakterien im Darm zu überprüfen. Sie müssen die wichtige Entscheidung treffen, ob Stoffe, die in unseren Körper gelangen, schädlich oder harmlos sind, ob sie also bekämpft werden müssen oder toleriert werden können.
Ergebnisse unserer und anderer Arbeitsgruppen zeigen, dass unabhängig voneinander sowohl ein Defekt der Epithelzellen als auch eine unregulierte Immunantwort zu einem Zusammenbruch des immunologischen Gleichgewichts im Darm führen. In der Folge können chronisch entzündliche Darmerkrankungen (Morbus Crohn und Colitis ulcerosa) entstehen. Eine weitere mögliche Folge unkontrollierter Immunreaktionen im Darm ist die Entstehung von Darmkrebs.
Apropos Darmflora: Die Darmflora eines Menschen, auch Mikrobiom genannt, besteht aus etwa 100 Billionen Bakterienzellen. Das übertrifft die Zellzahl des gesamten menschlichen Körpers um ein Vielfaches. Diese riesige Gemeinschaft von Mikroorganismen im Darm spielt eine entscheidende Rolle bei der Verdauung, der Produktion von Vitaminen und beeinflusst sogar unser Immunsystem und unser psychisches Wohlbefinden.
Ein spannendes Forschungsfeld ist auch das Nervensystem im Darm (enterisches Nervensystem). Es besteht aus über 100 Millionen Nervenzellen und wird oft als "zweites Gehirn" bezeichnet. Dieses weit verzweigte Netzwerk von Nervenzellen steuert nicht nur die Verdauung von der Peristaltik bis zur Enzymsekretion, sondern kommuniziert auch intensiv mit dem zentralen Nervensystem. Besonders interessant ist, dass das enterische Nervensystem auch eng mit dem Immunsystem des Darms interagiert, um Entzündungsprozesse zu modulieren, was eine entscheidende Rolle bei der Erhaltung der Gesundheit und der Prävention von Krankheiten spielt.
Das Darmepithel und dessen Bedeutung für den gesunden und erkrankten Darm
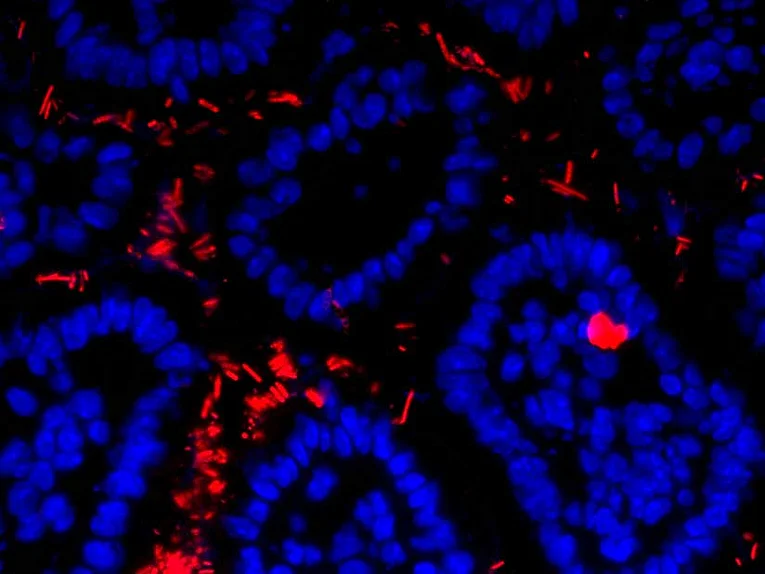
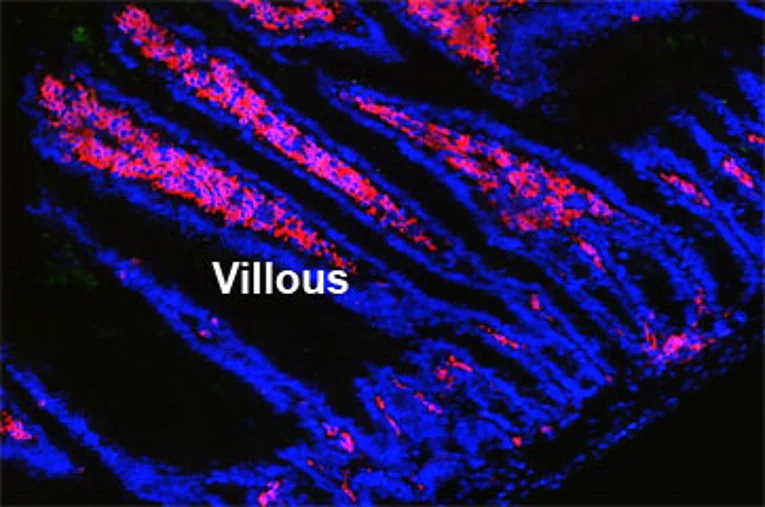
Der menschliche Darm beherbergt eine enorme Zahl von Bakterien (in der Abbildung rot gefärbt). Diese sind normalerweise unschädlich für den Körper und helfen sogar bei der Nahrungsverwertung. Wenn sie jedoch unkontrolliert in die Darmwand eindringen (einzelne rot gefärbte Zelle in der Abbildung links), können diese Bakterien gefährlich werden und Krankheiten verursachen. Daher ist die Darmoberfläche von einer dünnen Zellschicht so genannter Epithelzellen bedeckt (blau gefärbte Zellkerne aussen), die als Barriere wirken und die Bakterien vom Eindringen in die Darmwand abhalten. Epithelzellen sind hochspezialisierte Zellen. Sie bilden einerseits eine dichte Schutzschicht, andererseits produzieren sie zusätzlich Stoffe mit denen sie Bakterien auf Distanz halten oder gar abtöten können. Die Mechanismen, die diese Barriere – und somit einen gesunden Darm – erhalten, sind weitgehend unbekannt. Unser Forschungsteam widmet sich der Untersuchung dieser Mechanismen, die die Integrität dieser kritischen Barriere aufrechterhalten, ein Bereich, der bisher noch wenig erforscht ist.
Die Rolle der intestinalen Epithelzellen ist ebenfalls zentral in der Erforschung von Darmkrebs, da Tumore häufig aus diesen Zellen entstehen. Durch den Einsatz von molekularbiologischen Techniken und experimentellen Modellen zu Darmentzündungen und Darmkrebs untersuchen wir wichtige Signalwege wie STAT und NF-kappaB sowie die Prozesse der Proliferation, Differenzierung und des Zelltods in diesen Zellen. Diese Forschung trägt dazu bei, die komplexen Interaktionen im Darm zu verstehen und potenzielle Therapieansätze für Darmkrankheiten und Krebs zu entwickeln.
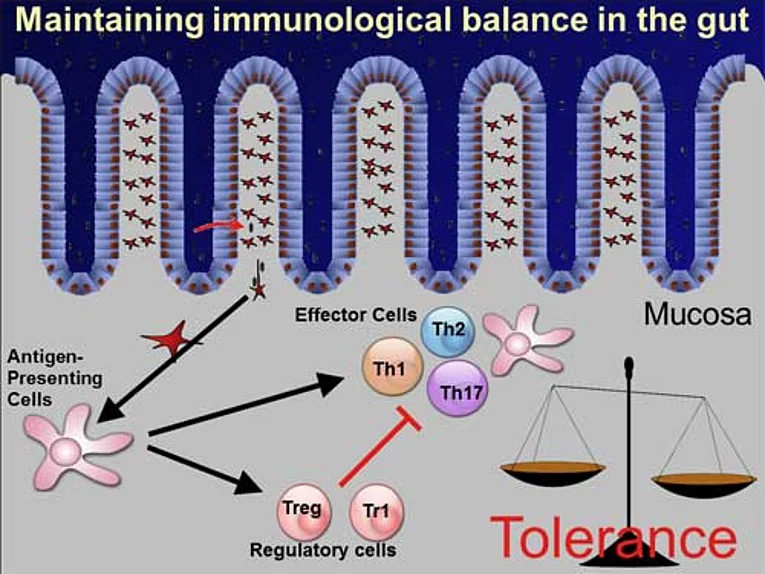
Der Darm ist das größte und vermutlich wichtigste Immunorgan des Körpers
Unterhalb der Epithelschicht des Darms liegt das größte Immunzelldepot des menschlichen Körpers. Die Immunzellen des Darms sind darauf spezialisiert pathogene Bakterien zu erkennen und zu bekämpfen. Diese Immunreaktion ist notwendig, um Gesundheit zu wahren, erzeugt jedoch auch Entzündungssymptome und Gewebeschädigung, wenn sie durch eindringende Bakterien ausgelöst wird. Um eine unkontrollierte Entzündung zu vermeiden, die durch Nahrungskomponenten oder harmlose Bakterien der Darmflora ausgelöst werden könnte, ist es essenziell, dass das Immunsystem des Darms eine Toleranz gegenüber diesen Elementen entwickelt. Hier spielen regulatorische T-Zellen, gefördert durch die Botenstoffe TGF-beta (Transforming Growth Factor beta) und Interleukin-10, eine Schlüsselrolle, indem sie das genetische Programm aktivierter T-Lymphozyten so modifizieren, dass diese zu toleranzfördernden Zellen werden. Die Erforschung der Toleranzmechanismen im Darm und deren Versagen bei chronischen Entzündungsprozessen ist ein zentrales Thema unserer Arbeitsgruppe.
Das Darmepithel als Kommunikationsschnittstelle zwischen Darmflora und Immunsystem
Das Darmepithel agiert als eine multifunktionale Schnittstelle zwischen dem Körper und seinem komplexen inneren Milieu, indem es sowohl als physische Barriere dient als auch als Vermittler zwischen der Darmflora und dem Immunsystem fungiert. Es erfasst Signale der Immunzellen und wandelt diese um in Befehle, die direkt die Zusammensetzung der Darmflora modifizieren können. Umgekehrt reagiert es auf Signale aus der Darmflora, und übersetzt diese in Signale, die vom Immunsystem verstanden werden und dieses beeinflussen, was zeigt, wie dynamisch die Interaktionen zwischen Darmepithel, Mikrobiom und Immunabwehr sind.
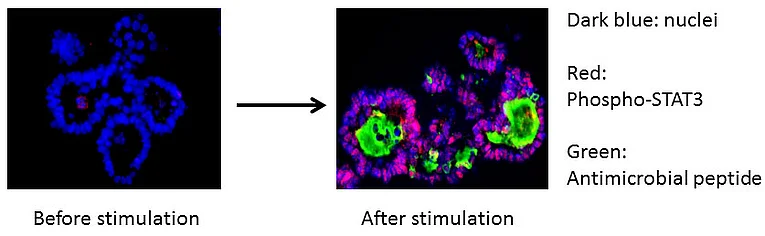
Ein Beispiel für diesen komplexen Signalverkehr ist die Reaktion des Darmepithels auf das Zytokin IL-22, das von Immunzellen im Darm produziert wird. IL-22 aktiviert in den Epithelzellen eine Signalkaskade, die den Transkriptionsfaktor STAT3 einschaltet. STAT3 wiederum fördert die Expression von REG3beta, einem antimikrobiellen Peptid, das von den Epithelzellen freigesetzt wird und eine wesentliche Rolle bei der Regulation der Darmflora spielt, indem es potenziell pathogene Bakterien bekämpft und die mikrobielle Balance erhält. Diese Wechselwirkungen sind entscheidend für die Aufrechterhaltung der intestinalen Homöostase und die Prävention entzündlicher Darmerkrankungen, was die Bedeutung des Darmepithels in der Immunregulation und der Erhaltung der Gesundheit unterstreicht.
Ausgewähle eigene Arbeiten zum Thema:
1) Bao et al. Epithelial OPA1 links mitochondrial fusion to inflammatory bowel disease. Science Transl Med. 2025. 17(781):eadn8699.
2) González-Acera et al. Integrated multi-model analysis of intestinal inflammation exposes key molecular features of preclinical and clinical IBD. Gut. 2025 Apr 29:gutjnl-2024-333729.
3) Gámez-Belmonte et al. Epithelial Presenilin-1 drives colorectal tumour growth by controlling EGFR-COX2 signalling. Gut. 2023. 72(6):1155-1166.
4) Patankar et al. E-type prostanoid receptor 4 promotes resolution of colitis by blocking intestinal epithelial necroptosis. Nature Cell Biol. 2021. 23(7):796-807.
5) Günther et al. Interferon lambda Promotes Paneth Cell Death via STAT1 Signaling in Mice and is Increased in Inflamed Ileal Tissues of Patients with Crohn’s Disease. Gastroenterology. 2019. 157(5):1310-1322
6) He et al. Regression of apoptosis-resistant colorectal tumors by induction of necroptosis in mice. J Exp Med. 2017. 214(6):1655-1662.
7) Günther et al. Caspase-8 controls the gut response to microbial challenges by TNFalpha -dependent and –independent pathways. Gut. 2015. 64(4):601-610
8) Wittkopf et al. Cellular FLICE-Like Inhibitory Protein Secures Intestinal Epithelial Cell Survival and Immune Homeostasis by Regulating Caspase-8. Gastroenterology. 2013. 145(6):1369-79.
9) Günther et al. Caspase-8 regulates TNF-alpha-induced epithelial necroptosis and terminal ileitis. Nature. 2011. 477(7364):335-9.
10) Pickert et al. STAT3 links IL-22 signalling in intestinal epithelial cells to mucosal wound healing. J. Exp. Med. 2009. 206(7):1465-72.
11) Nenci et al. Epithelial NEMO/IKK-gamma links innate immunity to chronic intestinal inflammation. Nature. 2007. 29;446(7135):557-61.
12) Becker et al. TGF-beta suppresses tumor progression in colon cancer by inhibition of IL-6 trans-signaling. Immunity. 2004. 21(4): 491-501.